
Unidad 5



5.3. Balanceo o ajuste de ecuaciones químicas



Las ecuaciones químicas siguen una serie de normas de escritura e interpretación que les permite tener un significado unívoco.
Estas normas son:

En el primer miembro escribimos los reactivos y en el segundo los productos. Si hay varios reactivos o varios productos, los separamos mediante el signo +
Separamos los dos miembros de la ecuación mediante una flecha que indica el sentido de la transformación

En la ecuación solo describimos el curso principal de la reacción. No constan los pa sos intermedios que pudieran tener lugar, solo el estado inicial (reactivos) y el final (productos).

Solo escribimos las sustancias que intervienen propiamente en la reacción. No hacemos constar, por ejemplo, el agua de disolución.
Frecuentemente, indicamos el estado físico de las sustancias que intervienen. Después de la fórmula añadimos los símbolos (s), (l), (g) y (aq).
En ocasiones, empleamos algunos símbolos para identificar otras características del proceso
El símbolo ∆, colocado sobre la flecha, indica el sentido de la transformación, significa ‘calentamiento’.
Una flecha junto a un producto significa ‘desprendimiento de gas’.
Una flecha junto a un producto significa ‘formación de un precipitado sólido’.

Métodos de ajuste de ecuaciones

La ecuación química también debe expresar las cantidades relativas de las sustancias que intervienen.
Si escribimos la reacción de descomposición del clorato de potasio:
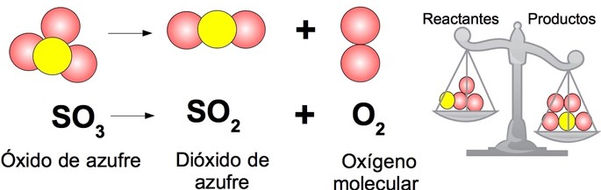
Observamos que el número de átomos de oxígeno que intervienen en la reacción no es el mismo en los reactivos que en los productos.
El problema se resuelve si colocamos, por ejemplo, el coeficiente fraccionario 3/2 delante de la fórmula del oxígeno:
A esta operación la denominamos ajustar o igualar una ecuación química. Ajustar una ecuación química consiste en asignar a cada fórmula un coeficiente ade cuado de modo que en los dos miembros haya el mismo número de átomos de cada elemento.

PERO ESO NO ES TODO EXISTEN OTROS MÉTODOS DE IGUALACIÓN

El método de tanteo
El método del sistema de ecuaciones
Método de balanceo ion - electrón
El método de tanteo se utiliza en ecuaciones sencillas. Consiste en aplicar el método de ensayo-error
Se emplea en los casos en que resulta más complicado asignar los coeficientes por tanteo. Consiste en plantear tantas ecuaciones como tipos de átomos intervienen en la reacción.
Es una forma de balancear ecuaciones químicas de reacciones redox (de transferencia de electrones), separando la reacción en dos partes: una donde se pierden electrones (oxidación) y otra donde se ganan electrones (reducción). Luego se igualan los electrones perdidos y ganados, y se juntan ambas partes para tener la ecuación balanceada.
Escanea los códigos y encontrarás más información

